Для развития промышленных аптечных пунктов нужно найти решение задачи доступности фармсубстанций в небольших фасовках. Министерство здравоохранения предложил регистрировать субстанции специально для экстемпоральных фармацевтических средств. Еще одна трудность — отсутствие спроса со стороны мед компаний.
Увеличение доступности фармсубстанций, которые включены в госреестр в целях выполнения, также вспомогательных веществ по нужной номенклатуре в небольших фасовках — это один из вопросов, волнующ?? промышленные аптеки. Про это на совещании рабочей группы по производству экстемпоральных препаратов Государственной Думы заявил депутат Айрат Фаррахов, передает журналист «ФВ».
Как добыть субстанции
Промышленным аптечным пунктам не хватает ассортимента фармсубстанций, 2-ая трудность — огромные фасовки, считает заместитель заведующего лабораторией регуляторных отношений Санкт-Питерского химфармуниверситета Дмитрий Юрочкин.
«Большая фасовка часто приводит к нерентабельности, производственная аптека не успевает в течение определенной степени применять данные лекарственные субстанции и обязана их перерабатывать», — подчеркнул он.
Юрочкин думает, что нужно провоцировать лекарственных производителей включать субстанции в список как ЕАЭС, так и в государственный, в связи с тем, что промышленные аптеки могут производить конкретно из лекарственных субстанций, которые включены в список, или из зарегистрированных фармацевтических препаратов.
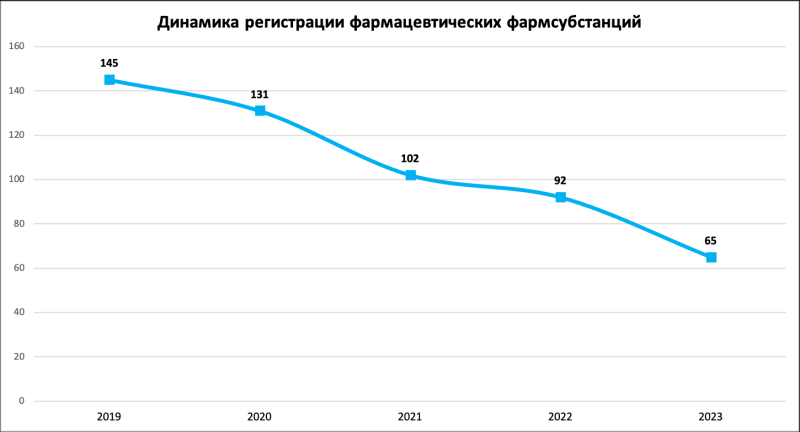
Заместитель министра здравоохранения Сергей Глаголев подчеркнул, что после вступления в силу законодательства ЕАЭС о едином эталоне регистрации фармацевтических средств, которое ввело довольно широкие требования к качеству как лекарственных субстанций, так и фармацевтических препаратов, уменьшилось число регистрируемых фармсубстанций.
При всем этом увеличилось число фармацевтических препаратов, выпускаем?? серийно на производстве. «Данный парадокс связан также с тем, что широкая промышленность низкомаржинальных дешевых аналогов, производимых с внедрением заграничных субстанций, при посредстве поставок участников биржевых торгов, сейчас уступает место локализации, сегментации этого рынка и развитию производства субстанций по полному циклу. Отталкиваясь от логики ЕАЭС, мы регистрируем большая часть субстанций в составе фармацевтических препаратов, и имеются точные регуляторные ограничения на выдергивание этой субстанции из досье и начало его вольной реализации», — сообщил заместитель министра.
Источник: ГРЛС
Он также сообщил, что лекарственные субстанции, используем?? в промышленных аптечных пунктах, должны региться как самостоятельные товары. Другими словами должен быть заявитель регистрации, «налаженный институт выпуска той либо другой серии в обращение, на базе протоколов изучения, подписанных уполномоченным по качеству».
Согласно мнению Глаголева, нужно узнать запрос промышленных аптечных пунктов на нужную номенклатуру фармсубстанций, чтоб промышленность производителей субстанций соображала, какие товары требуются для аптечных пунктов. «Отталкиваясь от этого, мы тоже проведем работу с Министерством промышленности и торговли по активизации регистрации данных товаров», — резюмировал Глаголев.
Вопрос небольших размеров субстанций, как он сообщает, можно решить методом делегирования промышленным аптечным пунктам фасовки для следующей перепродажи иным промышленным аптечным пунктам.
При всем этом пригодится решить вопросы обеспечения качества, входного и выпускающего контроля, установления срока годности.
Кому необходимы промышленные аптеки
2-ой вопрос, который обсуждался на совещании, — обеспечение спроса на медицинские препараты, сделанные в аптечных пунктах. «Трудность в том, что докторы разучились подписывать рецепты, и у нас все информационные мед системы в принципе не нацелены на работу с рецептурой», — сказал управляющий Ассоциации муниципальных аптечных пунктов Павел Ястребов. При всем этом спрос на подобные препараты у некоторых докторов все таки есть.
Руководитель по экономике здравоохранения «Р-Фарм» Александр Быков подчеркнул, что клинические советы не содержат распоряжений на то, чтоб можно было назначать персонально сделанные фармацевтические препараты, потому это не возместится ни ОМС, ни иными источниками выделения финансовых средств. Если Федеральная служба по надзору в сфере здравоохранения будет инспектировать, то нарушение клинических советов будет рассматриваться как нарушение условий по обеспечению качества медпомощи.
Руководитель Союза лекарственных и биомедицинских кластеров Захар Голант считает, что нужно развивать спрос на экстемпоральную рецептуру. «Если чрезвычайно-чрезвычайно грубо, всюду, где на данный момент написано зарегистрированный фармацевтический продукт, обязана показаться запятая, у нее обязана показаться экстемпоральная фармацевтическая форма. Это должно происходить и в системе ставок, и в системе льготного фармацевтического обеспечения», — сообщил он.