Качество методологических исследовательских работ препаратов, которые предлагаются к включению в списки ЖНВЛП и ВЗН, стало лучше с 2020 года по 2024 год. К данному заключению пришли специалисты ЦЭККМП Министерства здравоохранения РФ. Всего за обозначенный период изучили 168 фармацевтических средств.
Центр экспертных исследований и контроля качества медпомощи (ЦЭККМП) Министерства здравоохранения РФ проанализировал динамику методологического качества исследовательских работ фармацевтических средств, которые предлагаются к включению в списки, в рамках всеохватывающей оценки с 2020 года по 2024 год. Как рассказали в пресс-центре ЦЭККМП, всего за данное время провели всеохватывающую оценку для 167 фармацевтических препаратов, из них 123 — для включения в Список ЖНВЛП, 27 — в Список 14 ВЗН и 17 — в оба списка.
Специалисты отметили улучшение качества методологических исследовательских работ таких препаратов в анализируемом периоде:
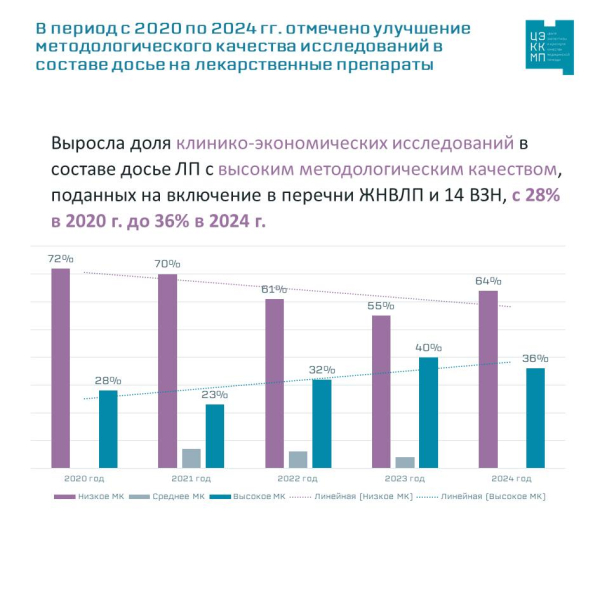
- с двадцати восьми процентов в 2020 году до тридцати шести процентов в 2024 году увеличился процент клинико-финансовых исследовательских работ в составе досье ЛП с высоким методологическим качеством, которые были поданы на включение в списки ЖНВЛП и 14 ВЗН;
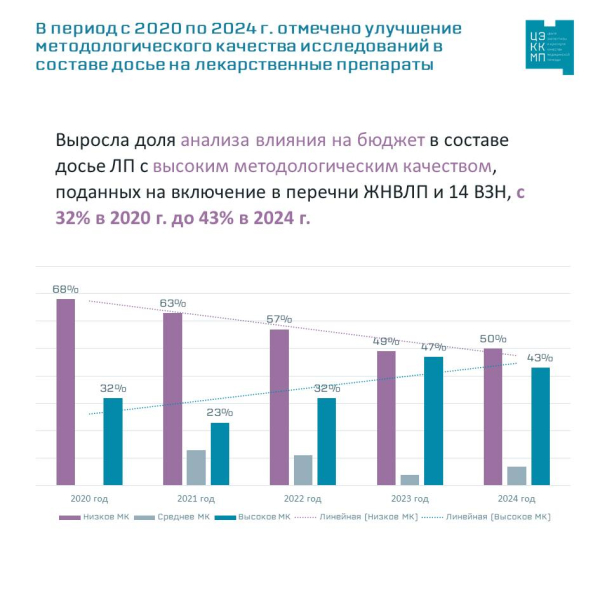
- с тридцати двух процентов в 2020 году до сорока трех процентов в 2024 году увеличился процент исследовательских работ изучения воздействия на бюджет в составе досье ЛП с высоким методологическим качеством, которые были поданы на включение в списки ЖНВЛП и 14 ВЗН.
Оценка методологического качества исследовательских работ препаратов, которые предлагаются к включению в списки, выведена в некоторый шаг всеохватывающей оценки с 2024 года. Объективность предоставляемых исследовательских работ (клинико-финансовых и изучения воздействия на бюджет) почти во всем зависит от их методологического качества. Чем выше качество исследовательских работ, тем больше степень доверия к приобретенным результатам.
| Всеохватывающей оценке фармацевтического продукта подвергаются клинико-экономическое исследование (КЭИ) и изучение воздействия на бюджет (АВБ), которые были предоставлены заявителем, также проводится изучение доп последствий, который учитывает сведения о госрегистрации предлагаемого ЛП, его обращении, также препаратов, которые включены в списки и имеют подобные показания к применению. |